针对病毒感染引起的传染病,为了明确致病的病毒种类,可以进行以下两类检查:
直接检测病毒本身:可以检测病毒表面的抗原,也可以检测病毒的核酸。
检测人体为了抵抗病毒产生的抗体。
通常情况下,抗原检测对实验室条件要求不高,主要适用于基层医院进行的大规模筛查;抗体检测操作方便,10~15分钟即可获得检测结果;而核酸检测则对实验室条件、检测人员、仪器要求高,但结果也最为准确和敏感。
截至目前,国家药品监督管理局共批准新冠病毒检测试剂15个,其中核酸检测试剂10个,抗体检测试剂5个,没有批准病毒抗原的相关检测。
下面,我们针对新冠病毒的核酸检测和抗体检测已获批的方法进行介绍。
传送门:病毒核酸检测
目前已批准的10个新冠病毒核酸检测试剂,有8个采用的都是荧光PCR法,剩余的检测方法分别是联合探针锚定聚合测序法和恒温扩增芯片法。
荧光PCR法
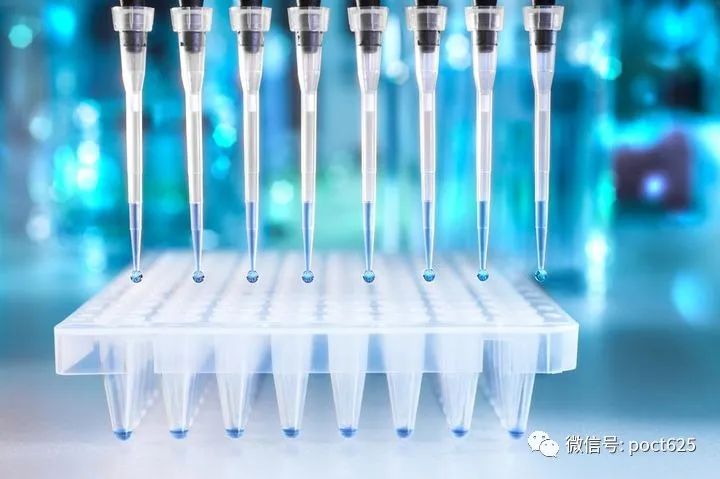
PCR法指的是聚合酶链式反应,能将微量的DNA大幅增加。用于检测新冠病毒时,由于新冠病毒是RNA病毒,需要先将病毒RNA逆转录为DNA,再进行PCR检测。
荧光PCR检测的原理为,随着PCR的进行,反应产物不断累积,荧光信号强度也等比例增加。最后通过荧光强度变化监测产物量的变化,从而得到一条荧光扩增曲线图。
这是目前新冠病毒核酸检测最常用的方法。但下列因素可能导致检测结果出现误差:
保存不当或未及时送检:RNA病毒很容易降解,因此,获得患者样本后,需要规范地保存,并尽快进行检测。否则,很可能导致检测结果不准确。
结果解读错误:目前批准的检测产品都是根据新型冠状病毒基因组中开放读码框1a/b、包膜蛋白和核衣壳蛋白进行选择。但不同产品的检测引物、探针设计存在不同,有单靶区段、双靶区段、三靶区段的检测和判读差别。因此,如果没有严格按照不同的说明书进行判读,有可能导致结果判断错误。
联合探针锚定聚合测序法
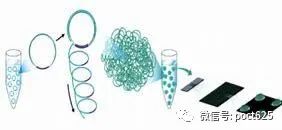
这种检测主要是用专门的仪器检测测序载片上DNA 纳米球携带的基因序列。
这种检测的灵敏度高,不容易漏诊,但结果也容易受多种因素的影响而不准,包括:
未及时检测样本:和荧光PCR法一样,如果没有规范保存和尽快检测,结果可能不准。
检测场所的室温过高:这也会影响检测结果的准确性。
不同的检测仪器、试剂盒也可能对结果造成影响。
恒温扩增芯片法

基因芯片检测是传统的病毒学诊断方法之一,检测原理是基于核酸之间的互补结合特性开发的一种检测方式,能够用于定性或定量测量存在于生物体内的核酸。和PCR相比,基因芯片准确率高,时间更短,但价格也更为昂贵、检测通量(单位时间内所能产生的数据量)相对更低。
此次获批的这个恒温芯片,能对新冠病毒在内的6种呼吸道病毒进行检测。1.5小时内便可获得结果,
和PCR相比,基因芯片准确率高,时间更短,但价格也更为昂贵、且检测通量(单位时间内所能产生的数据量)相对更低。
病毒抗体检测
抗体检测试剂是检测血清中由病毒进入人体后刺激人体产生的IgM或IgG抗体,IgM抗体出现较早,IgG抗体出现较晚。
目前已获批的5个新冠病毒抗体检测试剂,分别采用的是胶体金法和磁微粒化学发光法。
胶体金法
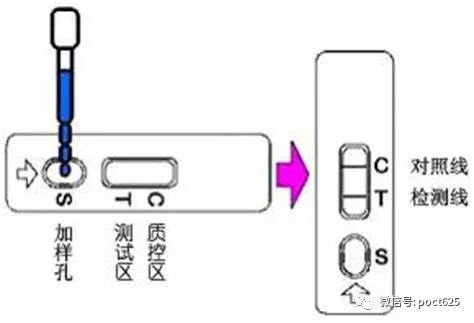
胶体金法是用胶体金试纸进行检测,也就是目前常说的快速检测试纸。
这种试纸经过特殊标记,上面有孔,用于滴入受检者的血清样本。胶体金试纸上面有2条线,一条叫做检测线,另一条叫做质量控制线,如果两条线都显色,代表阳性;只有质控线显色,代表阴性;这两种情况之外都属于无效结果。
这种检查一般在10~15分钟左右,就可以得出检结果。
这种检测方法很方便,出结果的速度也很快。但主要的不足在于,检测通量较低,有一定的误判率(主要是受抗体质量影响)。
而且,胶体金法检测的新冠病毒抗体是IgM抗体。IgM产生的时间要晚于病毒复制的时间,所以检测的时间窗口比核酸检测窄。
磁微粒化学发光法
化学发光法是一种高度敏感的免疫检测,凡具有抗原性的物质都可以用这种方法测定。
磁微粒化学发光法是在化学发光检测的基础上,加用了磁性纳米粒子,使检测具有了更高的灵敏度和更快的检测速度。
不过,磁微粒化学发光法选择性差,会对一个系列的化合物做出反应,而非特定的某一化合物,因此,准确性上相对不够好。而且,环境对检测的影响比较大,容易导致误差。
新冠核酸检测 vs 抗体检测,怎么选?
目前,指南推荐能用来确诊新冠病毒感染的仍然只有核酸检测。
对于新冠病毒核酸检测阴性的疑似病例,可以采用抗体检测作为补充检测指标。对于新冠病毒核酸检测的疑似病例,也可以用抗体检测来协同使用。
此外,抗体检测还可以发挥安全评估和疗效监测作用。例如,抗体检测可作为恢复期患者血浆治疗的监测评价,也可以用在疫苗研发和效价测定中。